STEMCELL Technologies StemSpan StemSpan Leukemic Cell Culture Kit
- 研究用
StemSpan™ Leukemic Cell Culture Kit(ST-09720)は、悪性細胞の in vitro での培養および増殖用に開発された無血清の培地キットで、慢性骨髄性白血病(CML)および急性骨髄性白血病(AML)のサンプルで性能を検証済みです。最適化されたプロトコルによって、がん細胞を増殖・培養し、薬物スクリーニングに使用できます。
本品は、無血清培地 StemSpan™ SFEM II(単品の商品コード:ST-09605)、StemSpan™ CD34+ Expansion Supplement(10倍濃縮、 同:ST-02691)、低分子化合物 UM729(同:ST-72332)*で構成されています。
* 以前のUM171(ST-72912)から変更されています。
製品の特長
StemSpan™ Leukemic Cell Culture Kitで、慢性/急性骨髄性白血病細胞を培養
- ヒト骨髄性白血病細胞の培養、増殖、および薬物スクリーニングに最適
- インプットしたCD34+ CML細胞およびAML細胞から、CD34+細胞をそれぞれ約65倍および約30倍に増殖
データ紹介
以下の実験では凍結保存した細胞を用いましたが、新鮮なサンプルでも同様の結果が予想されます。
また、低分子としてUM729の代わりにUM171を用いていますが、UM729(終濃度1 uM)でも同等の結果が期待されます。ただし、特定の条件で細胞増殖を最適化するには、さらに滴定が必要になる場合があります。UM171とUM729の比較データを含む詳細は、Fares et al. 2014を参照してください。
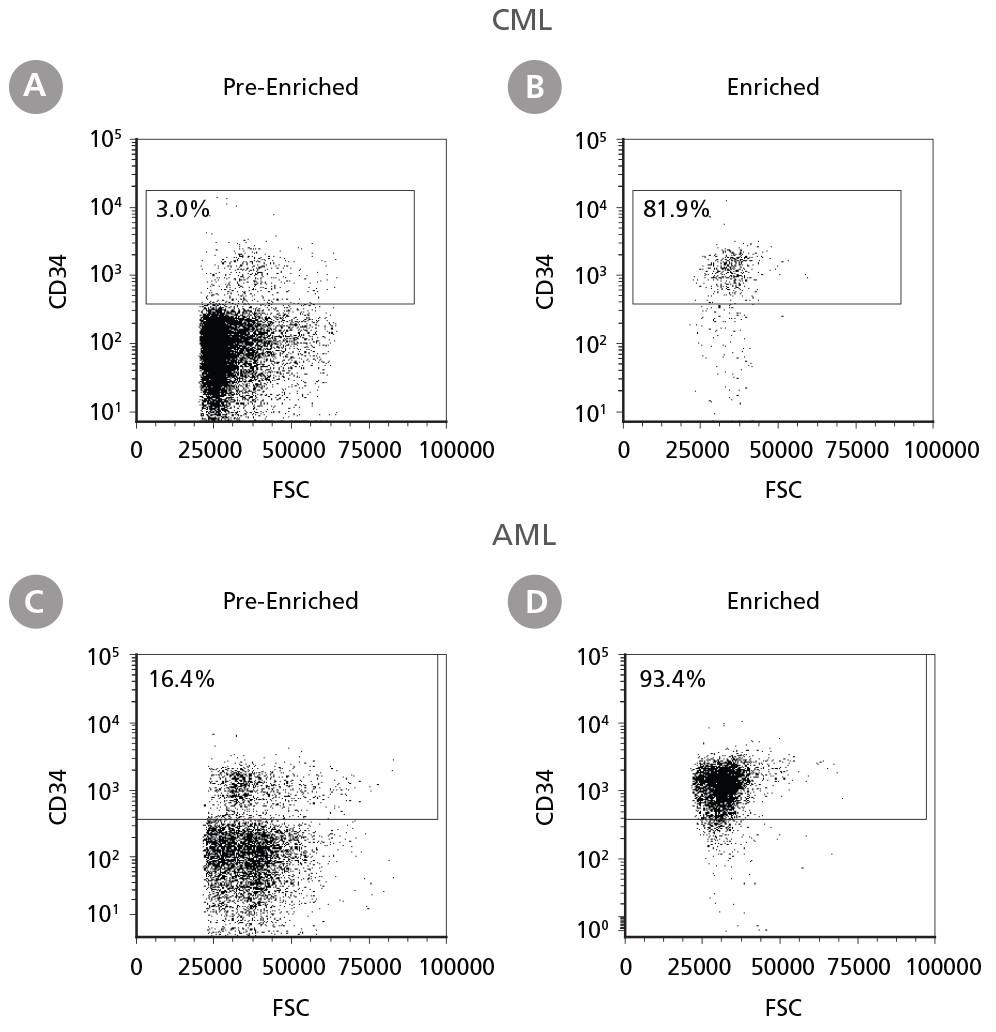
図1. 白血病ドナー由来CD34+細胞の分離
凍結保存したCMLまたはAMLの末梢血単核細胞(PBMC)および骨髄単核細胞(BMMC)を解凍し、細胞分離用に調製しました。EasySep™ Human Cord Blood CD34 Positive Selection Kit IIでCD34+細胞を分離しました。分離前(A, C)と後(B, D)のCD34+細胞の割合をフローサイトメトリーで測定しました。死細胞は光散乱プロファイルおよび生細胞染色で除外しました。この例では、CD34+細胞の純度は3%から82%(CML)および16%から93%(AML)にそれぞれ増加しました。
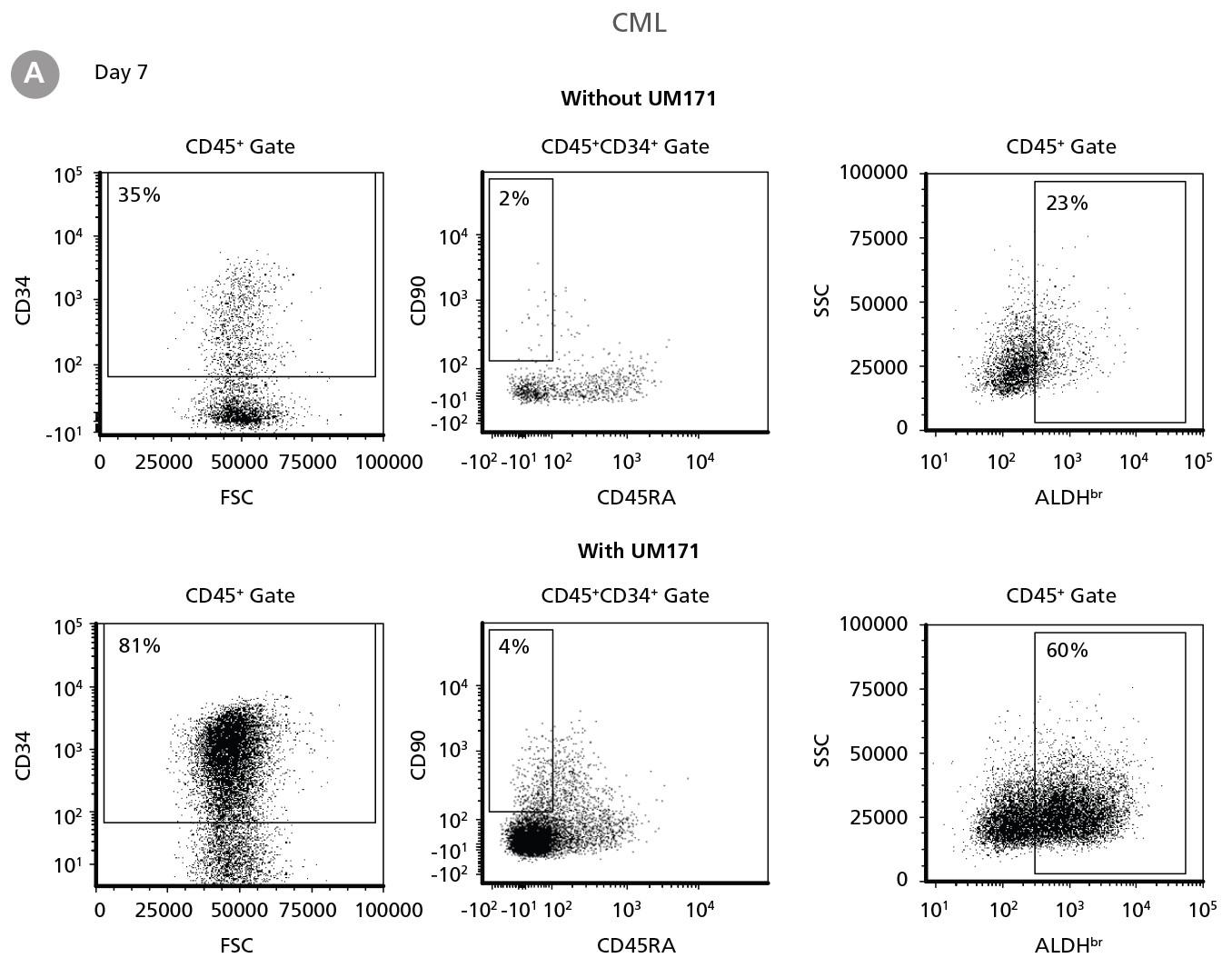
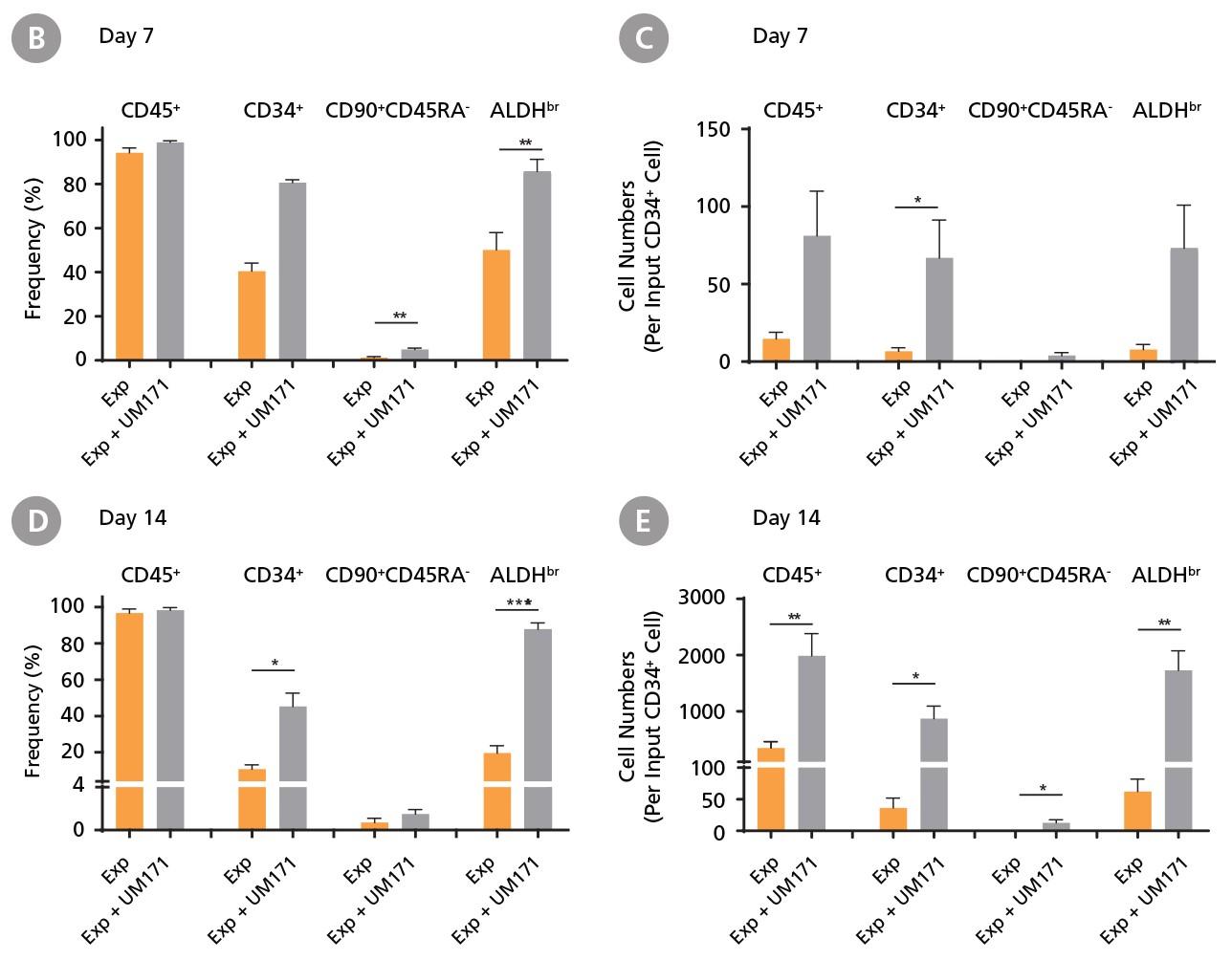
図2. CD34+ CML細胞の増殖
CD34+ CML細胞をUM171の添加有りまたは無しの条件下で、CD34+ Expansion Supplement(Exp)を添加したStemSpan™ SFEM IIで培養しました。培養7日後と14日後、培養細胞をCD45、CD34、CD90、CD45RAに対する蛍光標識抗体で染色し、ALDH活性測定のためALDEFLUOR™試薬(ST-01700)で染色し、フローサイトメトリーで分析しました。シーケンシャルゲートを使用して、CD45+、CD45+CD34+、CD45+CD34+CD90+CD45RA-生存細胞(「Fluorescence Minus One」(FMO)コントロールに基づく)、およびALDHbr細胞(DEABコントロールに基づく)の割合を決定しました。
(A)培養7日目の典型的なフローサイトメトリーのプロファイル。(B, C)培養7日目と(D, E)14日目のサブセットの(B, D)頻度と(C, E)最初のCD34+細胞あたりの細胞数。CD34+ Expansion Supplementを添加したStemSpan™ SFEM IIは、培養中のCML細胞の増殖をサポートします。UM171の追加により、調べた全サブセットの増殖が促進されました(UM171なしの培養と比較して、培養7日目でCD34+ 前駆細胞が10倍、14日目で20倍に拡大)。
データは平均値±SEM(n = 6)で表示。P値はtwo-tailed paired Student’s t-testで計算(* P <0.05; ** P <0.01; *** P <0.0001)。
調べた全6サンプルが培養・増殖できました。
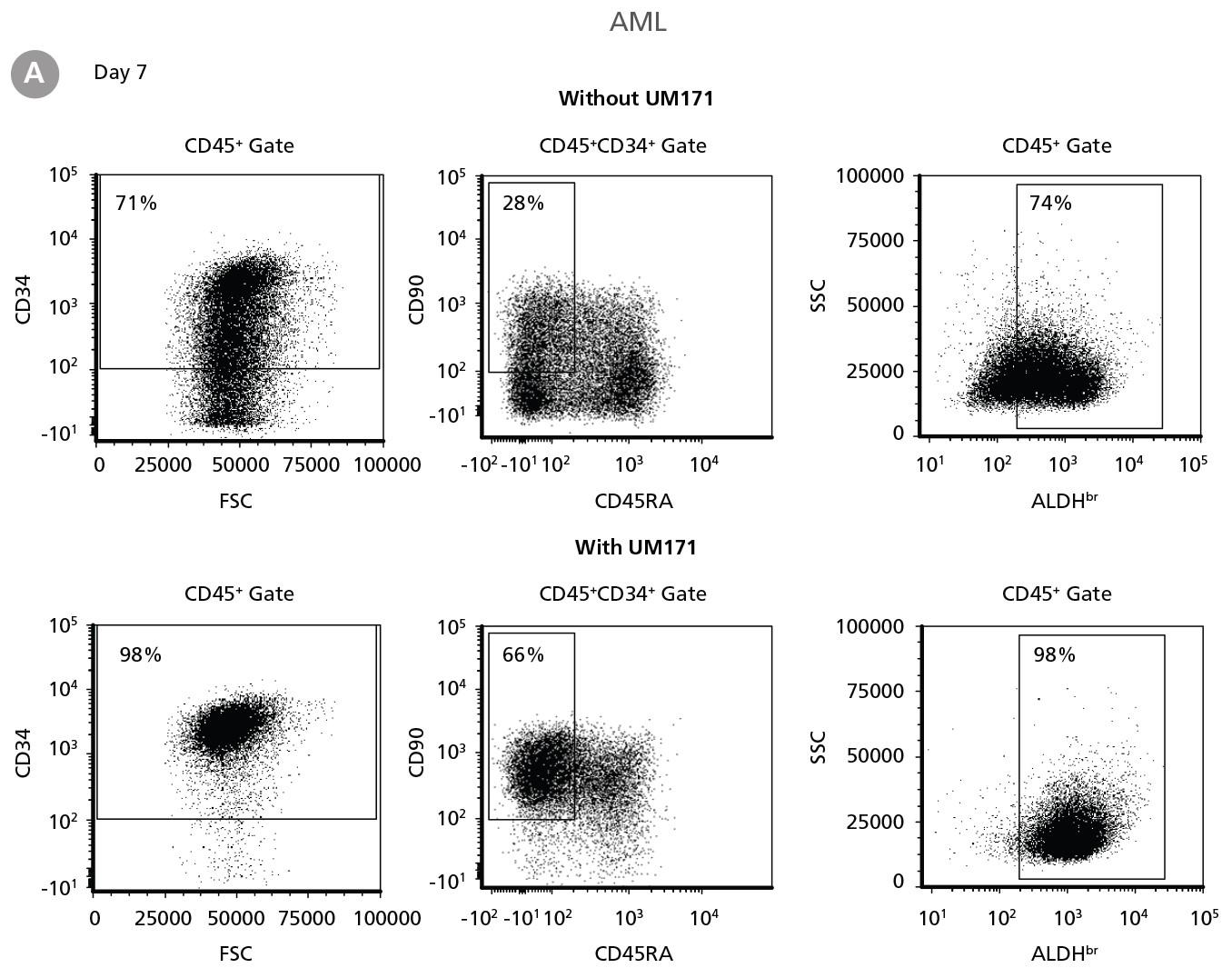
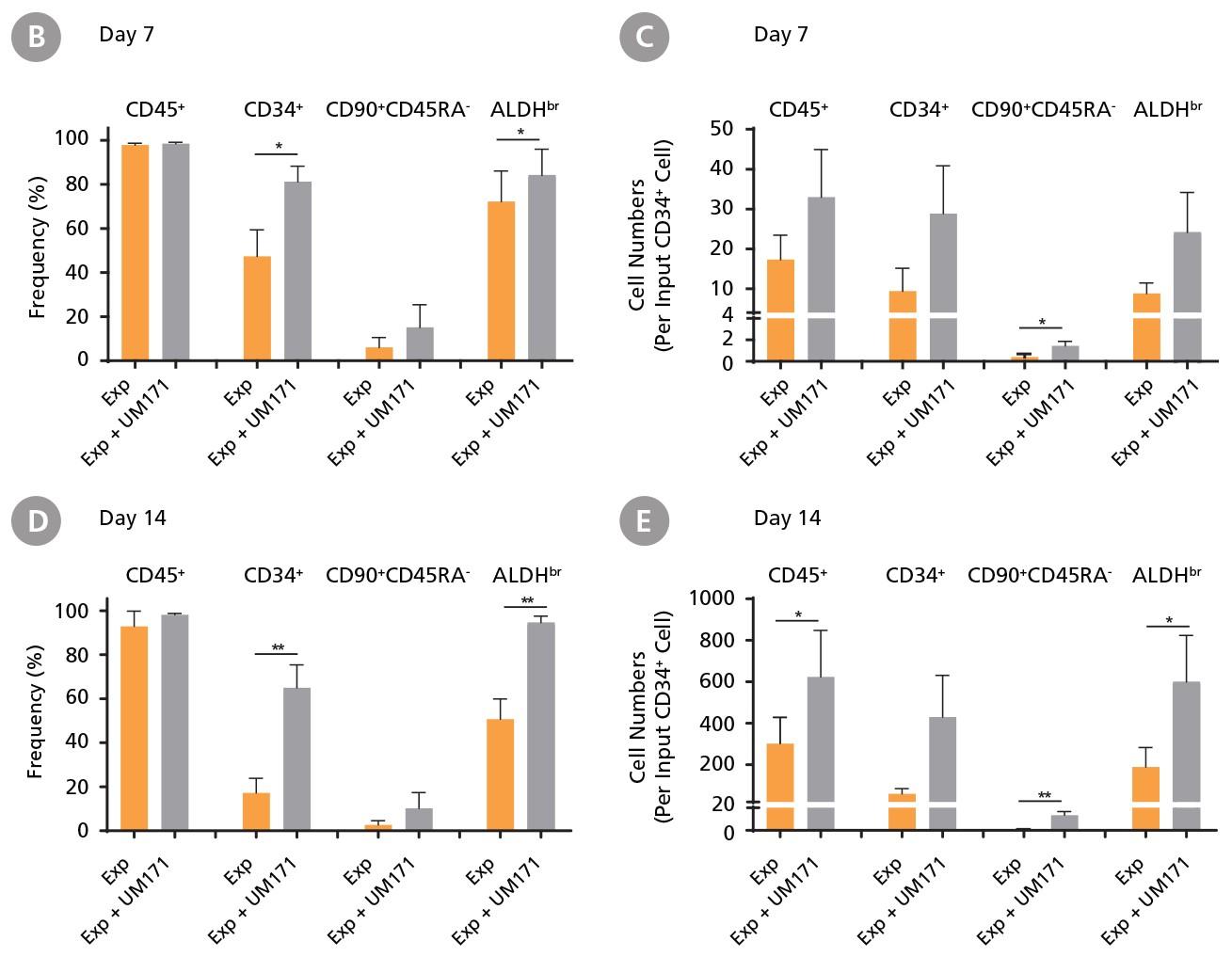
図3. CD34+ AML細胞の増殖
CD34+ AML細胞を、UM171の添加有りまたは無しの条件下で、CD34+ Expansion Supplement (Exp) を添加したStemSpan™ SFEM IIで培養しました。培養7日後と14日後、培養細胞を蛍光標識抗体とALDEFLUOR™(ST-01700)で染色しました。(A)7日目の代表的なフローサイトメトリープロファイル。(B, C)7日目および(D, E)14日目のサブセットの(B, D)頻度、および(C, E)最初のCD34+細胞あたりの細胞数。CD34+ Expansion Supplementを添加したSFEM IIは、培養中のAML細胞の増殖をサポートします。UM171を追加で添加すると、調べた全サブセットの増殖を促進します(UM171なしの培養と比較して、培養7日目にすべてのサブセットが3倍、14日目に7倍に拡大)。データは平均値±SEM(n = 6)で表示。P値は、two-tailed paired Student’s t-testで計算(* P <0.05; ** P <0.01)。 調べた全10サンプル中6サンプルが培養・増殖できました。
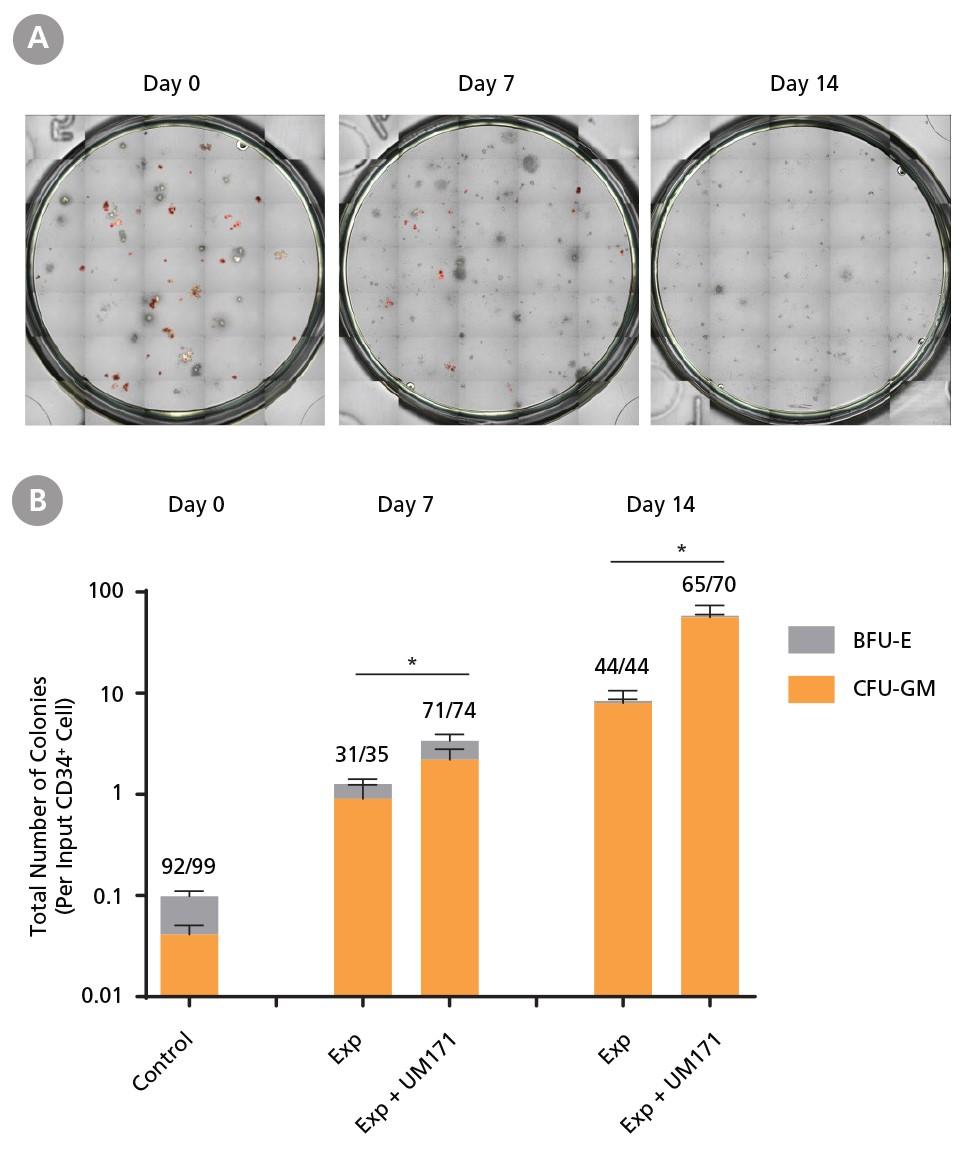
図4. CD34+ CML細胞のコロニー形成能の維持
CML細胞はCD34+細胞を分離直後(培養0日目)、またはCD34+ Expansion Supplement (Exp) を添加したStemSpan™ SFEM II(UM171添加有りまたは無し)で7日間または14日間増殖させた後(図2参照)、MethoCult™ H4435 Enriched培地に播種してコロニーアッセイしました。コロニーを(A)STEMvision™でデジタル画像化し、手動でカウントしました。(B)インプットしたCD34+細胞あたりのコロニー総数を表したCFUアウトプット。各バーの上にある数字は6つの異なるサンプル(個々の条件ごとに8〜12個のコロニーを採取)のqRT-PCRで測定したBCR-ABL陽性コロニーの割合を示します。CD34+ Expansion Supplementを添加したSFEM IIは、培養中のコロニー形成前駆細胞の増殖をサポートします。UM171の添加はコロニー形成前駆細胞のアウトプットをさらに促進します(7日目で約3.5倍、14日目で約8倍)。シングルコロニーqRT-PCR分析により、0日目サンプルから形成したコロニーと、7日間および14日間増殖させた細胞から形成したコロニーは主にBCR-ABL+でしたが、正常なBCR-ABL-前駆細胞もわずかに存在しました。データは平均値±SEM(n = 6)で表示。P値はtwo-tailed paired Student’s t-testで計算(* P <0.05)。
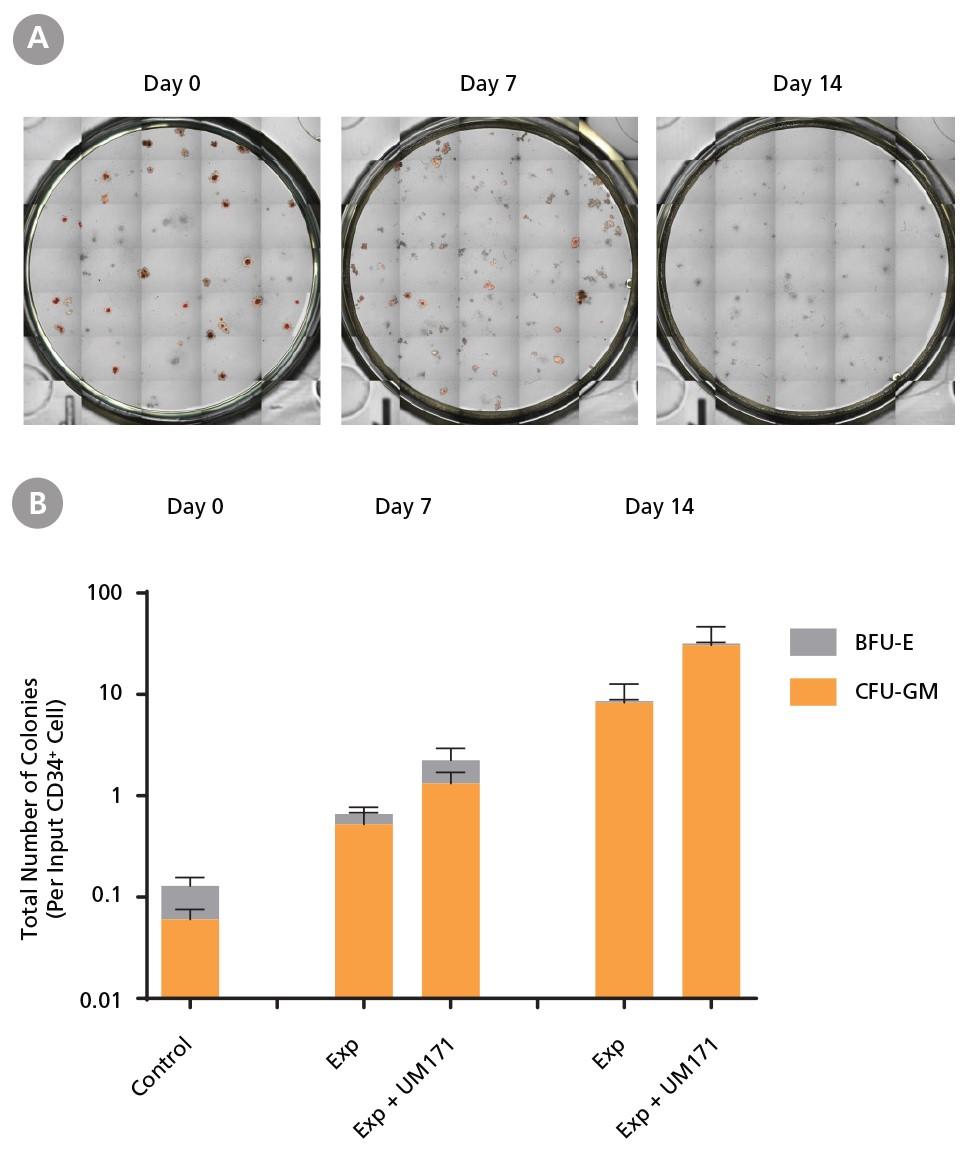
図5. CD34+ AML細胞のコロニー形成能の維持
AML細胞はCD34+細胞を分離後(培養0日目)、およびCD34+ Expansion Supplement (Exp) を添加したStemSpan™ SFEM II (UM171添加有りまたは無し)で7日間または14日間増殖させた後(図3参照)、MethoCult™ H4435 Enriched培地に播種してコロニーアッセイしました。コロニーを(A)STEMvision™でデジタル画像化し、手動でカウントしました。(B)インプットしたCD34+細胞あたりのコロニー総数で表したCFUアウトプット。CD34+ Expansion Supplementを添加したSFEM IIは、培養中のコロニー形成前駆細胞の増殖をサポートします。UM171の添加はコロニー形成前駆細胞のアウトプットをさらに促進します(培養7日目で約3倍、14日目で約4倍)。データは平均値±SEM(n = 6)で表示。P値はtwo-tailed paired Student’s t-testで計算(* P <0.05)。