研究者の声
2020/09/16
腸管オルガノイド培養をもちいた幹細胞競合のin vitro評価系を開発 研究者の声【25】
- 用途別細胞培養
今回ご紹介する研究室では放射線の生物影響に関する研究を行っていますが、最近マウス腸管オルガノイド培養をもちいて「幹細胞競合」を定量的に評価する方法を開発しました(Fujimichi et al., Sci Rep. 2019)。
このin vitro評価系によって、低線量・低線量率放射線の生物影響に対する理解が進むことが期待されます。
研究者紹介

ご紹介する論文
Fujimichi Y, Otsuka K, Tomita M, Iwasaki T. An Efficient Intestinal Organoid System of Direct Sorting to Evaluate Stem Cell Competition in Vitro. Sci Rep. 2019;9(1):20297.
研究内容
幹細胞競合とは、組織内で損傷細胞などの適応度のより低い細胞が細胞間の相互作用によって排除される「細胞競合」が、幹細胞間で生じることです。がんの原因となる異常な幹細胞を排除することによって、がん化を防ぐ機構としても注目されています。
今回、放射線照射および非照射のマウス小腸幹細胞を、それぞれ異なる蛍光で標識して混ぜ、混合オルガノイドとして培養しました。
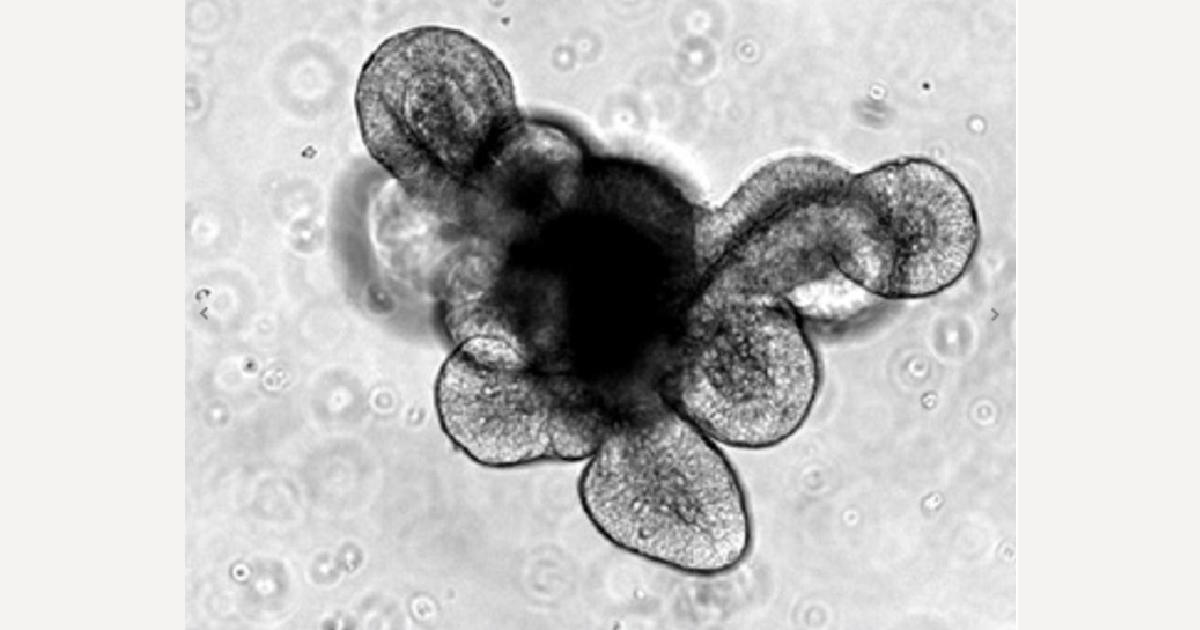
培養開始時の混合比を変えてオルガノイド内の幹細胞の占有率を調べたところ、放射線照射細胞の増殖が非照射細胞に比べて抑制されました(図1)。この結果は、放射線で誘発される幹細胞競合をin vitroで初めて再現するとともに、定量的に評価できることを示しています。
このことは、放射線の生物影響が、総線量が同じでも線量率が低くなると小さくなる現象(線量率効果)のメカニズムの1つが「細胞競合」であるという仮説を支持します。
オルガノイド培養を選んだ理由
組織内に放射線がヒットした細胞とヒットしなかった細胞が同時に混在するような低線量・低線量率放射線を直接マウスに照射しても、これらを区別して運命を追跡観察することは困難です。腸管オルガノイドは、培養しながら追跡観察が可能である点、着目する幹細胞がその他の細胞とクリプト様構造を形成し、細胞株と比べて生体に近い環境を構築できる点が魅力でした。このため、低線量・低線量率照射による生物影響解明のアプローチにオルガノイド培養が有効な手段であると考えました。
IntestiCultを選んだ理由
単一細胞に分離したマウス小腸幹細胞を6日間培養しオルガノイド形成効率(OFE)を調べたところ、Wnt3aおよびR-Spondin 1(RSPO1)を含有する条件培地と比べて、IntestiCult Organoid Growth Medium (Mouse)で顕著に高くなりました(図2)。
オルガノイド自体も出芽を伴う良い形態を示しました。そこで以降は培養にIntestiCultを用いることにしました。
論文中のIntestiCultに関するプロトコール
1)マウス腸管シングルセルの調製
Lgr5陽性幹細胞が緑色蛍光タンパク質EGFPで標識されるマウスの小腸(十二指腸)からクリプト部位を回収し、YTC(10 μM Y-27632, 2 μM Thiazovivin, 2.5 μM CHIR99021)を含むTrypLE Express で37℃、30分間処理して細胞を解離しました。細胞を40および20 μmのセルストレイナーに通し、2% FBSとYTCを含むPBS (−)に分散してシングルセルサスペンション(単一細胞懸濁液)を調製しました。
2)シングルセルからのオルガノイド培養と解析
V底型96ウェルプレートの各ウェルに、penicillin/streptomycin, N2, B27, EGF, N-acetylcysteine, Nogginを添加したIntestiCult Organoid Growth Medium (Mouse)と、YTCおよび1% Matrigelを加えておき、1)で調製したシングルセルからセルソーターでLgr5-EGFP幹細胞を分取しました。37℃のインキュベーター内で、3-4日ごとに新鮮培地を加えて培養しました。5-9日目に顕微鏡観察で形成されたオルガノイドを数え、9-11日目にオルガノイドをTrypLE Express + YTCで37℃、10分間処理してシングルセルに解離しフローサイトメトリーで解析しました。
オルガノイド/IntestiCultを使用した感想
当所では、10 mlずつのワーキングストックを作成し、利用しています。オルガノイド形成効率が良いので、実験系によっては少量の培地で充分な実験が行えます。一般的な細胞培養用の培地と比較して価格が高めではありますが、性能の点から使い続けていきたいと思っています。
今後の展望
今後は、オルガノイドの利点の1つである、in vitroでの生細胞イメージングに挑戦したいと考えています。オルガノイド中の幹細胞1個にマイクロビーム(放射線を細胞サイズ以下に絞ったビーム)を照射し、その照射幹細胞をタイムラプス観察することにより、照射幹細胞の運命追跡にも挑戦していきたいです。